Introducere
Durerea este o experiență universală, dar și profund personală. Doi pacienți cu aceeași fractură pot descrie senzații complet diferite: unul o suportă ușor, altul e copleșit de suferință. Mult timp, medicina a căutat explicația în factori anatomici sau psihologici. Însă cercetările din ultimii ani au dezvăluit un strat mai profund – epigenetica, limbajul invizibil prin care mediul, stresul și emoțiile rescriu expresia genelor.
Epigenetica durerii oferă o perspectivă fascinantă: suferința nu e doar un răspuns la un stimul, ci rezultatul unei „memorii biologice” create în celulele nervoase. Această memorie poate fi activată, amplificată sau chiar transmisă generațional. Durerea, astfel, devine un fenomen biologic și biografic – influențat de tot ce trăim, gândim și mâncăm.
Ce înseamnă epigenetica
Epigenetica („epi” = deasupra, „genetică” = referitor la gene) se ocupă cu modificările reversibile ale expresiei genelor, fără alterarea structurii ADN-ului. Practic, ADN-ul rămâne același, dar „citirea” lui se schimbă în funcție de factorii de mediu.
Principalele mecanisme epigenetice sunt:
- Metilarea ADN-ului, adică adăugarea unui grup metil (CH₃) pe secvențele de ADN, care „închide” anumite gene.
- Modificările histonelor, proteinele care înfășoară ADN-ul, controlând cât de „strâns” e împachetat și, implicit, cât de accesibil.
- ARN-urile necodificatoare, molecule care reglează fin activitatea genelor implicate în inflamație, durere sau regenerare tisulară.
Epigenetica funcționează ca un pian genetic: aceleași clape (genele) există la toți, dar mediul decide ce melodie se cântă.
Cum controlează epigenetica percepția durerii
Durerea apare atunci când receptorii nociceptivi din piele, mușchi sau organe sunt activați și trimit semnale către creier. Dar între stimul și percepție, intervin sute de gene care reglează sensibilitatea acestor neuroni.
Când un factor extern – stres, inflamație, traumă -modifică expresia acestor gene, apare ceea ce numim sensibilizare centrală: creierul devine „setat” să simtă mai multă durere, chiar și în absența unui stimul major.
De exemplu:
- metilarea crescută a genei OPRM1 (care codifică receptorii opioizi μ) reduce capacitatea organismului de a modula durerea în mod natural;
- hipometilarea genei COMT duce la degradarea rapidă a dopaminei și creșterea sensibilității la durere;
- modificări la nivelul genei BDNF (brain-derived neurotrophic factor) pot menține circuitele durerii active, chiar după vindecare.
Astfel, durerea cronică nu mai este doar o „leziune care nu se vindecă”, ci o expresie epigenetică persistentă.
Durerea acută și durerea cronică: două entități diferite
Durerea acută este un mecanism protector: avertizează asupra unei agresiuni și dispare după vindecare.
Durerea cronică, în schimb, devine un program biologic disfuncțional. Cercetările arată că pacienții cu durere cronică dezvoltă modificări epigenetice în regiuni cheie ale sistemului nervos central: talamus, cortexul insular și măduva spinării.
Aceste modificări afectează genele implicate în:
- neuroinflamație – prin activarea microgliei, celulele imunitare ale creierului;
- transmisia GABA–ergică, care inhibă durerea (scăderea activității GAD1 și GAD2 duce la hiperexcitabilitate neuronală);
- plasticitatea sinaptică, ceea ce face ca neuronii durerii să devină „super-reactivi”.
Rezultatul: corpul se comportă ca și cum ar fi rănit, deși rana nu mai există.
Când mediul rescrie codul durerii
Epigenetica e un traductor între viață și biologie.
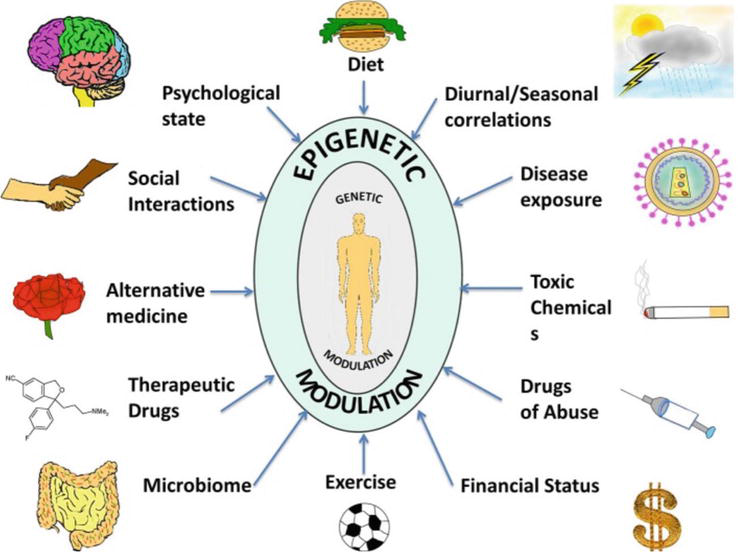
Cei mai importanți factori care pot schimba „codul durerii” sunt:
- Stresul cronic – nivelurile crescute de cortizol influențează metilarea genelor responsabile de axa hipotalamo–hipofizo–suprarenaliană. În timp, stresul rescrie modul în care corpul reacționează la durere, amplificând-o.
- Traumele emoționale timpurii – studiile arată că experiențele adverse din copilărie modifică expresia genei NR3C1, implicată în reglarea cortizolului. Copiii abuzați dezvoltă, la maturitate, o reactivitate crescută la durere.
- Dieta – carențele de metil-donori (folat, B12, colină) reduc capacitatea organismului de a regla epigenetic inflamația.
- Somnul insuficient – scade expresia genelor implicate în repararea neuronală și crește inflamația sistemică.
- Sedentarismul – duce la dereglarea epigenetică a genei IL6, crescând producția de citokine proinflamatorii.
Cu alte cuvinte, fiecare alegere zilnică devine un mesaj molecular către genele durerii.
Durerea transmisă generațional
Poate fi suferința moștenită? Da — nu în sensul metaforic, ci biologic.
Experimente pe animale au arătat că puii născuți din mame expuse la stres cronic prezintă hipersensibilitate la durere, chiar dacă nu au fost supuși aceluiași stres.
Modificările epigenetice la nivelul spermei și ovulelor pot transmite predispoziția la inflamație și sensibilitate nervoasă.
La oameni, studiile pe veteranii de război și copiii lor au arătat același fenomen: genele implicate în controlul stresului și durerii au semne epigenetice similare.
Durerea devine, astfel, o amprentă biologică a traumei.
Terapiile epigenetice — rescrierea suferinței
Medicina modernă începe să trateze durerea nu doar cu antiinflamatoare sau opioide, ci cu molecule care acționează asupra expresiei genelor.
Printre cele mai promițătoare direcții:
- Inhibitorii de histon-deacetilază (HDACi) – blochează enzimele care „închid” genele antiinflamatoare, reducând hipersensibilitatea neuronală.
- Agoniștii receptorilor nucleari PPAR – reglează expresia genelor implicate în inflamația cronică.
- Psihobioticele – bacterii probiotice care influențează epigenetic axa intestin–creier și pot reduce percepția durerii.
- Tehnicile de neuromodulare – precum stimularea magnetică transcraniană (TMS), care reactivează circuitele neuronale „închise” epigenetic.
Viitorul medicinii durerii este unul personalizat: analiza profilului epigenetic al pacientului ar putea permite alegerea tratamentului perfect pentru „codul său genetic activ”.
Stilul de viață: cea mai accesibilă terapie epigenetică
Epigenetica nu se modifică doar prin medicamente.
Obiceiurile zilnice pot „rescrie” expresia genelor durerii:
- Mișcarea regulată crește expresia genelor antiinflamatoare și a factorului BDNF, favorizând regenerarea neuronală.
- Alimentația antiinflamatoare (bogată în pește, legume, fructe de pădure, turmeric, ulei de măsline) reduce metilarea genelor proinflamatorii.
- Mindfulness și meditația scad activitatea genelor legate de stres și durere, efect dovedit în studii pe expresia NR3C1.
- Somnul profund restabilește echilibrul epigenetic al genelor care controlează inflamația.
Epigenetica ne oferă libertatea de a fi propriul nostru „editor genetic”. Fiecare alegere, de la ceea ce mâncăm la modul în care respirăm, influențează cum corpul nostru simte durerea.
Concluzie
Epigenetica durerii deschide un nou capitol în medicină: acela în care suferința nu mai e doar un simptom, ci o expresie biologică a experiențelor noastre.
Durerea cronică nu înseamnă doar nervi inflamați, ci și gene „rămase aprinse” prea mult timp.
Înțelegerea mecanismelor epigenetice oferă speranța unei terapii care nu doar ameliorează, ci rescrie durerea — la nivel molecular, profund și durabil.
În viitor, medicii nu vor întreba doar „unde doare?”, ci „ce gene au învățat să te doară?”.
Și poate, prin știință, nutriție și echilibru mental, vom învăța nu doar să tratăm durerea, ci să o dezactivăm chiar din rădăcina ei genetică.